Эксперт по сдаче вступительных испытаний в ВУЗах
Лабораторная работа № 5
ХРОМ. МАРГАНЕЦ
1 Теоретическая часть
Хром представляет собой твердый блестящий металл, плавящийся при 1890 ˚С; плотность его 7,19 г/см
3. У него достраивается d — подуровень предпоследнего слоя. В силу стабильности конфигурации d
5 у атомов хрома и молибдена наблюдается проскок одного электрона с оболочки ns на оболочку (n-1)d. У атомов хрома валентная электронная конфигурация 3d
54s
1. Внешняя электронная оболочка содержит один электрон, что обусловливает металлический характер этого элемента. Максимальная степень окисления равна +6, так как, помимо наружных электронов, в образовании связей может участвовать еще соответствующее число электронов из недостроенной предпоследней оболочки. Для хрома также характерны степени окисления +2,+3.
Соединения хрома (VI) отличаются неустойчивостью в растворах и являются сильными окислителями. При этом они чаще всего восстанавливаются до анионных или катионных комплексов хрома (III). Наиболее устойчивой степенью окисления хрома является +3. Это связано с тем, что соединения хрома (III) являются, как правило, комплексными с координационным числом 6 и октаэдрической пространственной конфигурацией расположения лигандов.
При комнатной температуре хром стоек к воде и к кислороду воздуха. Поверхность его покрывается оксидной пленкой, препятствующей коррозии.
Хром образует три оксида: оксид хрома (II) CrO, имеющий основной характер, оксид хрома (III) Cr
2O
3, проявляющий амфотерные свойства, и оксид хрома (VI) CrO
3– кислотный оксид.
В водных растворах соли хрома гидратированы и содержат комплексный катион [Cr(H
2O)
6]
3+, который обусловливает фиолетовую окраску. При нагревании растворов соли хрома CrCl
3*6H
2O часть координационной воды обменивается на хлорид-ионы (гидратная изомерия):
[Сr(Н
2О)]
6Cl
3 ↔ [СrС1(Н
2O)
5]Cl
2*Н
2О ↔ [СrС1
2(Н
2O)
4]С1*2Н
2О
фиолетовый зеленый темно-зеленый
Н
2СrО
4 — xромовая кислота, образующая соли хроматы. Н
2Сr
2О
7 — двухромовая кислота, ее соли — дихроматы. Как хромовая, так и двухромовая кислоты неустойчивы, однако их соли более прочны. В водных растворах хромат- и дихромат–ионы образуют равновесную систему:
Сr
2O
72− + Н
2О ↔ 2СrO
42− + 2Н
+
Отсюда следует, что в кислой среде равновесие смещено влево, в результате хромат превращается в дихромат, а при разбавлении водой или в щелочной среде – вправо и в результате дихромат переходит в хромат. Переход хромата в дихромат и наоборот можно наблюдать по изменению цвета окраски раствора.
Хроматы и дихроматы – сильные окислители, особенно в кислой среде.
Марганец, технеций и рений входят в VII-В подгруппу периодической системы и завершают первые пятерки вставных декад d-элементов. Их валентная электронная конфигурация (n-1)d
5ns
2. Имея на внешней электронной оболочке атома всего два электрона, марганец и его аналоги не способны присоединять электроны и в отличие от галогенов, соединений с водородом не образуют. Высшая степень окисления у них равна +7.
Для марганца наиболее характерны степени окисления +2 , +4, +7, относительно легко получаются производные, отвечающие степеням окисления 0, +3, +5, +6. Относительно стабильна степень окисления +2, поскольку наполовину заполненная d-оболочка отличается повышенной устойчивостью.
Марганец – серебристо-белый твердый хрупкий металл. Его плотность 7,44 г/см
3, температура плавления 1245 ˚С.
В ряду напряжений марганец находится между алюминием и цинком: стандартный электродный потенциал Mn/Mn
2+= − 1,18 В. На воздухе марганец покрывается тонкой защитной оксидной пленкой, предохраняющей его от дальнейшего окисления даже при нагревании. Но в мелкораздробленном состоянии марганец окисляется довольно легко. Вода при комнатной температуре действует на марганец очень медленно, при нагревании – быстрее. Марганец вытесняет водород из разбавленных кислот. Однако концентрированную серную кислоту он восстанавливает до оксида серы (IV), а азотную — до оксида азота (II); при этом образуются катионы Mn
2+.
Марганец образует четыре простых оксида: MnO, Мn
2O
3, обладающие основными свойствами, MnO
2— амфотерный, Мn
2O
7— ангидрид марганцовой кислоты НMnO
4.
Оксид марганца МnО нерастворим в воде, поэтому гидроксид марганца (II) получают действием щелочей на соли двухвалентного марганца, выпадает белый осадок гидроксида марганца. На воздухе гидроксид марганца (II) быстро темнеет, окисляясь в бурый гидроксид марганца (IV).
В практическом отношении наиболее важны соединения маргнца (II), диоксид марганца и соли марганцовой кислоты- перманганаты.
Перманганаты – сильные окислители. Степень окисления марганца в реакциях изменяется в зависимости от pН-среды:
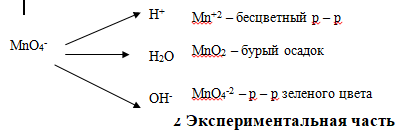 Опыт 1 Получение и свойства гидроксида хрома (III)
Опыт 1 Получение и свойства гидроксида хрома (III)
Получить в двух пробирках малорастворимый гидроксид хрома (Ш) взаимодействием 3-4 капель раствора соли хрома (III) с 1-2 каплями 2н раствора щёлочи NaOH. Испытать отношение гидроксида хрома (II) к кислотам и к избытку щёлочи, для чего добавить в одну пробирку по каплям 2н раствор щёлочи, в другую 2н раствор серной кислоты до растворения осадка.
Написать уравнения реакций, учитывая, что при взаимодействии гидроксида хрома (III) с избытком щелочи получается комплексный анион [Сr(ОН)
6]
3-.
Опыт 2 Восстановительные свойства солей хрома (III)
Получить раствор К
3[Сr(ОН)
6] добавлением к раствору соли хрома (III) избытка щёлочи (как в опыте 1), добавить в пробирку 3–4 капли 3%-ного раствора пероксида водорода. Нагреть смесь пламенем спиртовки до перехода зелёной окраски в желтую, что указывает на образование в растворе хромата калия.
Написать уравнение реакции окисления К
3[Сr(ОН)
6] в хромат калия.
Опыт 3 Влияние среды на смещение равновесия между хроматом и дихроматом
3.1 Переход хромата калия в дихромат
К 3–4 каплям раствора хромата калия прибавлять по каплям 2н раствор серной кислоты. Отметить изменение окраски раствора и указать, какими ионами эти окраски обусловливаются.
Написать уравнение реакции. Почему полученная соль относится к солям изокислот?
3.2 Переход дихромата в хромат
К 3–4 каплям раствора дихромата калия прибавлять по каплям раствор щелочи NaOH до изменения окраски.
Написать уравнение реакции. В какую сторону сместится равновесие:
2СrO
42− + 2Н
+ = Сr
2O
72− + H
2О
при добавлении: а) кислоты; б) щёлочи. Какой ион — СrO
42− или Сr
2О
72− существует в растворах: а) при pH < 7, б) при pH > 7?
Опыт 4 Окислительные свойства дихроматов
К 4-5 каплям раствора дихромата калия, подкисленного серной кислотой, добавить 3-4 капли раствора иодида калия. Отметить изменение окраски. Доказать выделение свободного йода, для чего в пробирку капнуть 1-2 капли раствора крахмала.
Отметить все наблюдаемые явления. Написать уравнения реакций.
Опыт 5 Кислотно-основные свойства гидроксида марганца (II)
В две пробирки внести по 3-4 капли раствора соли марганца (II) и по 2-3 капли 2н раствора щёлочи NaOH. Какой цвет полученного осадка гидроксида марганца (II)? Размешать осадок стеклянной палочкой и отметить его побурение вследствие окисления марганца (II) до Мn (IV). Во вторую пробирку с осадком гидроксида марганца добавить 2-3 капли 2н раствора серной кислоты. Что наблюдается?
Какие свойства характерны для гидроксида марганца (II)?
Написать уравнения реакций:
а) получение гидроксида марганца (II);
б) окисление его кислородом воздуха до гидроксида марганца (IV);
в) взаимодействие гидроксида марганца (II) с серной кислотой.
Опыт 6 Восстановительные свойства соединений марганца (II)
Поместить в пробирку 1-2 капли раствора соли марганца (II) и 5-6 капель 2н раствора азотной кислоты. Добавить на кончике микрошпателя висмутата натрия NаBiO
3. Как изменилась окраска раствора?
Как изменилась степень окисления марганца? Написать уравнение реакции, протекающей с образованием марганцовой кислоты и нитрата висмута (III).
Опыт 7 Окислительные свойства соединений марганца (VII). Влияние рН-среды на характер восстановления перманганат-иона
В три пробирки внести по 3-4 капли раствора перманганата калия. В одну пробирку добавить 2 капли 2н раствора серной кислоты, в другую- столько же воды, в третью- 3-4 капли 2н раствора щёлочи NaOH. Во все три пробирки прибавить по 1 микрошпателю кристаллического сульфита натрия или калия.
Отметить различные изменения первоначальной окраски раствора перманганата в каждом случае. Чем это вызвано? Написать уравнения реакций.
Ссылка на первоисточник:
http://www.axu.ru/

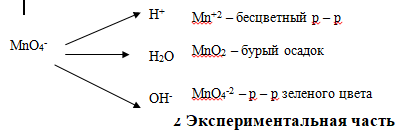 Опыт 1 Получение и свойства гидроксида хрома (III)
Получить в двух пробирках малорастворимый гидроксид хрома (Ш) взаимодействием 3-4 капель раствора соли хрома (III) с 1-2 каплями 2н раствора щёлочи NaOH. Испытать отношение гидроксида хрома (II) к кислотам и к избытку щёлочи, для чего добавить в одну пробирку по каплям 2н раствор щёлочи, в другую 2н раствор серной кислоты до растворения осадка.
Написать уравнения реакций, учитывая, что при взаимодействии гидроксида хрома (III) с избытком щелочи получается комплексный анион [Сr(ОН)6]3-.
Опыт 2 Восстановительные свойства солей хрома (III)
Получить раствор К3[Сr(ОН)6] добавлением к раствору соли хрома (III) избытка щёлочи (как в опыте 1), добавить в пробирку 3–4 капли 3%-ного раствора пероксида водорода. Нагреть смесь пламенем спиртовки до перехода зелёной окраски в желтую, что указывает на образование в растворе хромата калия.
Написать уравнение реакции окисления К3[Сr(ОН)6] в хромат калия.
Опыт 3 Влияние среды на смещение равновесия между хроматом и дихроматом
3.1 Переход хромата калия в дихромат
К 3–4 каплям раствора хромата калия прибавлять по каплям 2н раствор серной кислоты. Отметить изменение окраски раствора и указать, какими ионами эти окраски обусловливаются.
Написать уравнение реакции. Почему полученная соль относится к солям изокислот?
3.2 Переход дихромата в хромат
К 3–4 каплям раствора дихромата калия прибавлять по каплям раствор щелочи NaOH до изменения окраски.
Написать уравнение реакции. В какую сторону сместится равновесие:
2СrO42− + 2Н+ = Сr2O72− + H2О
при добавлении: а) кислоты; б) щёлочи. Какой ион — СrO42− или Сr2О72− существует в растворах: а) при pH < 7, б) при pH > 7?
Опыт 4 Окислительные свойства дихроматов
К 4-5 каплям раствора дихромата калия, подкисленного серной кислотой, добавить 3-4 капли раствора иодида калия. Отметить изменение окраски. Доказать выделение свободного йода, для чего в пробирку капнуть 1-2 капли раствора крахмала.
Отметить все наблюдаемые явления. Написать уравнения реакций.
Опыт 5 Кислотно-основные свойства гидроксида марганца (II)
В две пробирки внести по 3-4 капли раствора соли марганца (II) и по 2-3 капли 2н раствора щёлочи NaOH. Какой цвет полученного осадка гидроксида марганца (II)? Размешать осадок стеклянной палочкой и отметить его побурение вследствие окисления марганца (II) до Мn (IV). Во вторую пробирку с осадком гидроксида марганца добавить 2-3 капли 2н раствора серной кислоты. Что наблюдается?
Какие свойства характерны для гидроксида марганца (II)?
Написать уравнения реакций:
а) получение гидроксида марганца (II);
б) окисление его кислородом воздуха до гидроксида марганца (IV);
в) взаимодействие гидроксида марганца (II) с серной кислотой.
Опыт 6 Восстановительные свойства соединений марганца (II)
Поместить в пробирку 1-2 капли раствора соли марганца (II) и 5-6 капель 2н раствора азотной кислоты. Добавить на кончике микрошпателя висмутата натрия NаBiO3. Как изменилась окраска раствора?
Как изменилась степень окисления марганца? Написать уравнение реакции, протекающей с образованием марганцовой кислоты и нитрата висмута (III).
Опыт 7 Окислительные свойства соединений марганца (VII). Влияние рН-среды на характер восстановления перманганат-иона
В три пробирки внести по 3-4 капли раствора перманганата калия. В одну пробирку добавить 2 капли 2н раствора серной кислоты, в другую- столько же воды, в третью- 3-4 капли 2н раствора щёлочи NaOH. Во все три пробирки прибавить по 1 микрошпателю кристаллического сульфита натрия или калия.
Отметить различные изменения первоначальной окраски раствора перманганата в каждом случае. Чем это вызвано? Написать уравнения реакций.
Опыт 1 Получение и свойства гидроксида хрома (III)
Получить в двух пробирках малорастворимый гидроксид хрома (Ш) взаимодействием 3-4 капель раствора соли хрома (III) с 1-2 каплями 2н раствора щёлочи NaOH. Испытать отношение гидроксида хрома (II) к кислотам и к избытку щёлочи, для чего добавить в одну пробирку по каплям 2н раствор щёлочи, в другую 2н раствор серной кислоты до растворения осадка.
Написать уравнения реакций, учитывая, что при взаимодействии гидроксида хрома (III) с избытком щелочи получается комплексный анион [Сr(ОН)6]3-.
Опыт 2 Восстановительные свойства солей хрома (III)
Получить раствор К3[Сr(ОН)6] добавлением к раствору соли хрома (III) избытка щёлочи (как в опыте 1), добавить в пробирку 3–4 капли 3%-ного раствора пероксида водорода. Нагреть смесь пламенем спиртовки до перехода зелёной окраски в желтую, что указывает на образование в растворе хромата калия.
Написать уравнение реакции окисления К3[Сr(ОН)6] в хромат калия.
Опыт 3 Влияние среды на смещение равновесия между хроматом и дихроматом
3.1 Переход хромата калия в дихромат
К 3–4 каплям раствора хромата калия прибавлять по каплям 2н раствор серной кислоты. Отметить изменение окраски раствора и указать, какими ионами эти окраски обусловливаются.
Написать уравнение реакции. Почему полученная соль относится к солям изокислот?
3.2 Переход дихромата в хромат
К 3–4 каплям раствора дихромата калия прибавлять по каплям раствор щелочи NaOH до изменения окраски.
Написать уравнение реакции. В какую сторону сместится равновесие:
2СrO42− + 2Н+ = Сr2O72− + H2О
при добавлении: а) кислоты; б) щёлочи. Какой ион — СrO42− или Сr2О72− существует в растворах: а) при pH < 7, б) при pH > 7?
Опыт 4 Окислительные свойства дихроматов
К 4-5 каплям раствора дихромата калия, подкисленного серной кислотой, добавить 3-4 капли раствора иодида калия. Отметить изменение окраски. Доказать выделение свободного йода, для чего в пробирку капнуть 1-2 капли раствора крахмала.
Отметить все наблюдаемые явления. Написать уравнения реакций.
Опыт 5 Кислотно-основные свойства гидроксида марганца (II)
В две пробирки внести по 3-4 капли раствора соли марганца (II) и по 2-3 капли 2н раствора щёлочи NaOH. Какой цвет полученного осадка гидроксида марганца (II)? Размешать осадок стеклянной палочкой и отметить его побурение вследствие окисления марганца (II) до Мn (IV). Во вторую пробирку с осадком гидроксида марганца добавить 2-3 капли 2н раствора серной кислоты. Что наблюдается?
Какие свойства характерны для гидроксида марганца (II)?
Написать уравнения реакций:
а) получение гидроксида марганца (II);
б) окисление его кислородом воздуха до гидроксида марганца (IV);
в) взаимодействие гидроксида марганца (II) с серной кислотой.
Опыт 6 Восстановительные свойства соединений марганца (II)
Поместить в пробирку 1-2 капли раствора соли марганца (II) и 5-6 капель 2н раствора азотной кислоты. Добавить на кончике микрошпателя висмутата натрия NаBiO3. Как изменилась окраска раствора?
Как изменилась степень окисления марганца? Написать уравнение реакции, протекающей с образованием марганцовой кислоты и нитрата висмута (III).
Опыт 7 Окислительные свойства соединений марганца (VII). Влияние рН-среды на характер восстановления перманганат-иона
В три пробирки внести по 3-4 капли раствора перманганата калия. В одну пробирку добавить 2 капли 2н раствора серной кислоты, в другую- столько же воды, в третью- 3-4 капли 2н раствора щёлочи NaOH. Во все три пробирки прибавить по 1 микрошпателю кристаллического сульфита натрия или калия.
Отметить различные изменения первоначальной окраски раствора перманганата в каждом случае. Чем это вызвано? Написать уравнения реакций.